Sentraalinen Sensitaatio ja Migreeni
Mitä CS tarkoittaa?
Sentraalien sensitaatio (Central Sensitization, CS) on alunpitäen nimitys fysiologiselle eli normaalille hermojärjestelmän viestinkuljetusmekanismille äärihermosta selkäytimen kautta aivoihin. Aivoja voidaan ajatella ikään kuin kovalevynä, jonne tallentuu muistoja, kokemuksia ja tapahtumia, niin hyvässä kuin pahassa. Aivot muistuttavat meitä erilaisten kipusignaalien avulla asioista, joita tulisi välttää. Normaali (fysiologinen) kiputuntemus on suojarefleksi, sen tehtävänä on ilmoittaa kudosvauriosta tai tulehduksesta. Normaaliin kiputuntemukseen kuluu esimerkiksi salamannopea havaitseminen ja kivun paikantamisen kyky. Lisäksi kivun aistimiseen liittyy analysointi kivun tai muun tuntemuksen luonteesta: onko se vaarallista, epämiellyttävää tai miellyttävää. Nämä aistimukset laukaisevat refleksikaaria, esimerkiksi lihasliikkeen, väistörefleksin tai tunnereaktion.
Joskus kuitenkin aivot alkavat ylireagoida ärsykkeisiin, tilanteisiin ja tuntemuksiin, jolloin kipuviestit voimistuvat ja alkavat toistua yhä useammin, uudelleen ja uudelleen. Tällöin kiputuntemus on vääristynyt (epäfysiologinen). Viime vuosina sentraalinen sensitaatio -termiä on käytetty kuvaamaan epäfysiologiseksi voimistunutta ja vääristynyttä hermoston toimintaa. Sentraalinen sensitaatio tarkoittaakin hermosolujen virittymistilaa, joka ylittää normaalit fysiologiset tarpeet ja aiheuttaen monia toiminnanhäiriöitä. Jos normaali tunto- tai kipuaistimus kulkee äärihermoja myöten ensin selkäytimeen ja sieltä useamman, viestiä monella tavalla muokkaavan sekä analysoivan aivorunkorakenteen kautta aivokuorelle aistittavaksi, sentraaliseksi sensitisaatioksi kutsuttu ilmiö sen sijaan voi vääristää tätä viestiketjua sen kaikilla tasoilla. Tällöin kipuviesti vahvistuu, kulkeutuu anatomisesti tavanomaista laajemmalle alueelle -jopa täysin erilaista aistimusta viestittävään hermoon. Stimuluksen jälkeen aktivaatio säilyy poikkeuksellisen pitkään ja on aktivoitavissa taas uudelleen vähäisenkin ärsykkeen voimasta tai se voi jopa aktivoitua itsekseen. Sentraalinen sensitaatio ja siihen liittyvät ilmiöt muuttavat kipuaistien toimintaa, mm. vääristämällä, lisäämällä, pitkittämällä ja laajentamalla kiputuntemuksia, mutta myös tuomalla esille kivun aistimista ilman äärihermon vauriota tai tulehdusta. Kipuaistimus on aito, mutta sen elimistöä suojaava funktio puuttuu tai sitä ei enää ole, tällöin taustalta puuttuu ” elimellinen sairaus”.
Tällöin voi kehittyä krooninen kiputila, johon liittyy myös kivun aistimuksen toisen tärkeän osan eli laadun ja merkittävyyden aistimisen muutos. Mukana on siis aivojen tunnepuolta säätelevän alueen, limbisen järjestelmän sensitaatiota, joka helposti aiheuttaa ahdistuksen ja masennuksen kaltaisia mielialan muutoksia. Hyvin mielenkiintoinen kliininen havainto on, että ahdistusoiretta voi provosoida esille myös ns. kivun ekvivalenttioireet. Näitä CSS:lle tyypillisiä sensoriikan eli tuntohermotuksen vääristymiä ovat puutuminen, pistely tai paineen tunne.
Mitä CSS tarkoittaa?
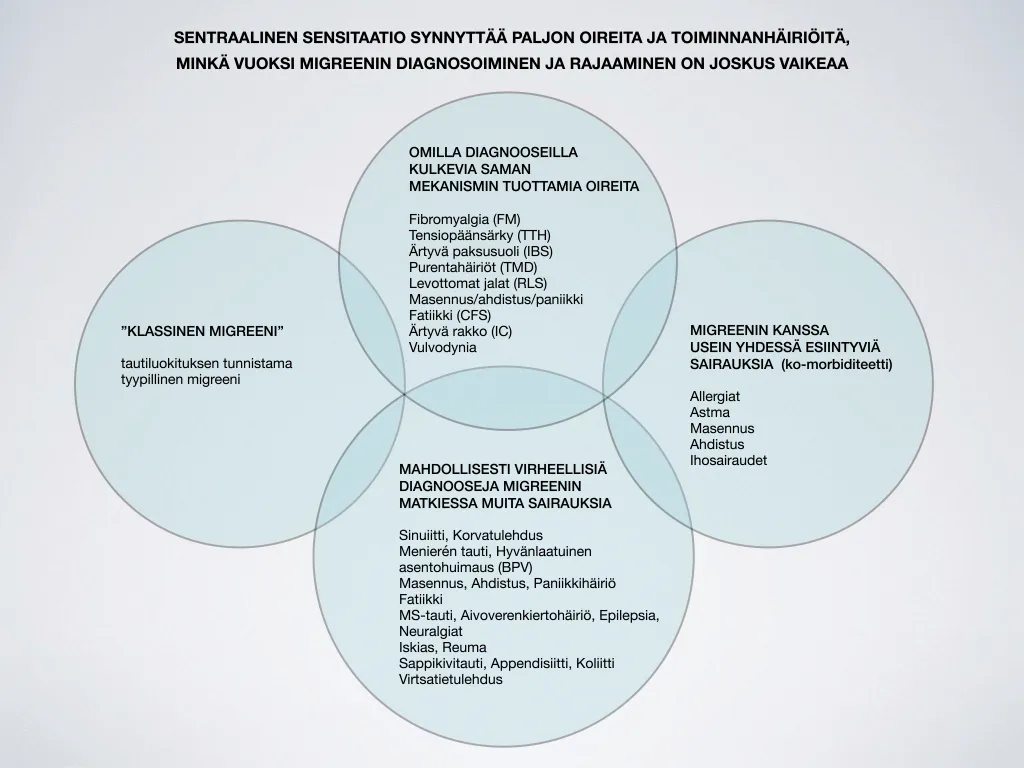
Useisiin kroonisiin kiputiloihin, joissa ei ole elimellistä sairautta taustalla, ajatellaan liittyvän sentraalinen sensitaatiomekanismi. Kroonisiin kiputiloihin liittyy myös paljon muuta sairastuvuutta eli ko-morbiditeettia. Epidemiologisten tutkimusten sekä kliinisen kokemuksen perusteella on selvää, että tietyt usein mekanismiltaan epäselvät tai toiminnalisiksi häiriöiksi tulkitut sairaudet kasaantuvat samoille henkilöille. On luontevaa ajatella, että ainakin osittain näitä sairauksia yhdistää sama taustamekanismi eli sentraalinen sensitaatio.
Sentraalinen sensitaatio oireyhtymä (Central Sensitivity Syndrome, CSS) / Sentraalinen sensitaatio (tai sensitiviteetti) syndrooma tarkoittaa monioireista sairautta tai joukkoa sairauksia, joiden taustamekanismina on voimistunut ja vääristynyt hermoston toiminta eli sentraalinen sensitaatio.
Historiallisista syistä tämän oireyhtymän nimikkeen alle kuuluu monia eri tauteja , joko oirediagnooseja tai aiemmin mekanismiltaan huonosti tunnettuja kuvailevia oireyhtymiä eli syndroomia.
Sentraalinen sensitaatiomekanismi ja migreeni
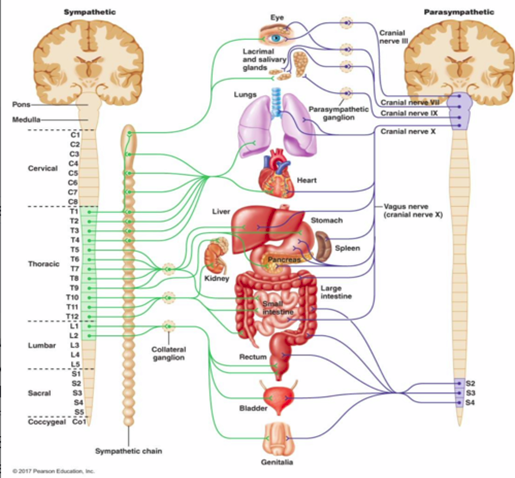
CS – mekanismin ymmärtäminen on oleellista, että voidaan ymmärtää miten migreenin oireet syntyvät ja miten monella tavalla migreeni voi oireilla: miksi pää tai mikä tahansa kehon osa voi olla kipeä tai puutunut, miksi suoli, rakko, sydän tai keuhkot toimivat oudosti, miksi mieliala heittelee, muisti ja keskittyminen pätkii, väsyttää eikä lihaksetkaan toimi.
CS ja CSS eri lääketieteen alojen näkökulmasta
Oma huomioni on , että nyt käsiteltävä teema, sentraalinen sensitaatio, on eri viitekehityksestä eli lääketieteen eri erikoisaloilta katsottuna, ymmärretty tai sovellettu eri tavoin. Kun aiheesta on kirjoitettu esimerkiksi kipututkijoiden tai kipupotilaiden kanssa työskentelevien kliinikoiden kuten reumatologien tai fysiatrien toimesta, saattaa tarkastelunäkökulma ja päätelmät poiketa neurologien ja varsinkin migreenin kanssa työskentelevien tavasta käsitellä aihetta. Asian voisi kiteyttää niin, että esimerkiksi kipututkimuksen alalla sentraalinen sensitaatio -termi on yleistynyt käyttökielen ilmaisuksi kuvattaessa kipuaistumuksen muuttumista ja vääristymistä keskushermostossa ja sen pohjalta on pohdittu mitä kliinisiä ilmentymiä, sairaus-fenotyyppejä se selittäisi.
Reumatologien lähestymistapa julkaisuissa on usein fibromyalgiaan (FM) liittyvä ko-morbiditeetti eli mitkä sairausdiagnoosit siihen yleisimmin korreloivat. Näitä ovat mm. päänsärky, masennus, väsymys ja ärtynyt paksuoli. Näiden eri sairauksien yhteinen yhdistävä mekanismi tunnistetaan sentraaliseksi sensitaatioksi, mutta migreeniä näissä patogeneettisissä pohdiskeluissa ei nosteta esille juuri koskaan. Migreenin kannalta katsottuna ne monet sairausdiagnoosit joita pidetään osana sentraalista sensitaatio syndroomaa (CSS) ovat vain laajakirjoisen kroonistuneen migreenin oireita ja niitä on kuvattu kirjallisuudessa jo kauan ennen kuin koko CS – mekanismia on tunnettu.
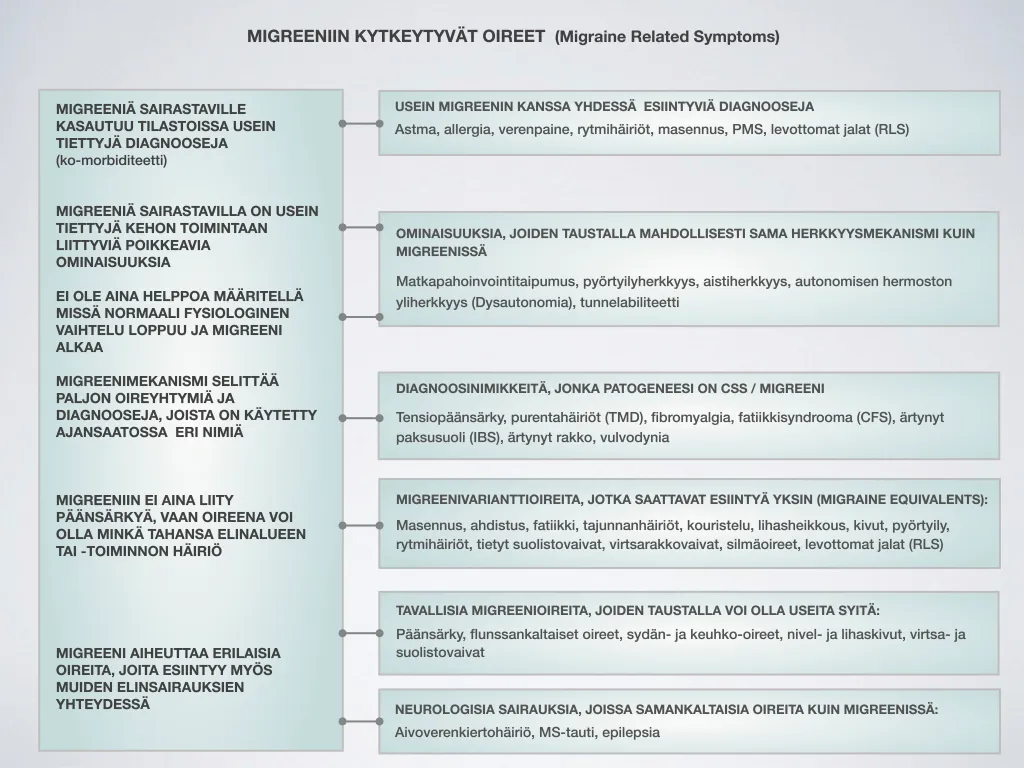
Neurologisesta näkökulmasta CSS-sairaudet voidaan tulkita kahdella tavalla: joko ”perinteisesti ” krooniseen migreeniin liittyviksi ko-morbidi-sairauksiksi tai niin, että ne ovat itsessään migreenioireita tai migreenin ”ekvivalenttioireita”. Tämä näkemys perustuu teoriaan, jonka mukaan migreenin patogeneesi on sentraalinen sensitaatio ja sen kroonistuessa syntyy kroonisia oireita, jotka saavat erilaisia kuvailevia diagnoosinimiä.
Migreenin kirjoitettu historia on pitkä ja tarkkoja kuvauksia tästä monioireisesta sairaudesta onkin jo vuosisatojen takaa. Näissä kuvatut migreeniin liittyvät ”liitännäis-” tai ”ekvivalentti”-oireet on helposti tunnistettavissa SSS – ryhmän oireiksi ja diagnooseiksi. Migreenillä on tässä nimeämis/ nomenklatuuri- asiassa erityisasema myös seuraavista syistä: se on vahvasti perinnöllinen, oireilu puhkeaa yleensä jo varhaisella iällä (toisin kuin muut CSS- ryhmän diagnoosit) ja siihen liittyy pitkäaikaista perustutkimusta niin genetiikan, neurobiologian kuin epidemiologiankin osalta. Migreenimekanismin teorioissa, luokittelussa ja hoidoissa keskiössä oli aiemmin aivoverisuonet, mutta nykyään hermosolujen sensitaatiomekanismilla on keskeinen rooli. Migreenille on tyypillistä ajassa ja henkilöstä toiseen laajasti vaihteleva oirekuva. Anatomisesti SS -mekanismin sijainti vaihtelee ja se voi vääristää aistimuksia ja muuta hermosäätelyä missä tahansa keskushermoston ja äärihermojen alueilla. Oire voi olla laaja, koko kehon yleisoireilu tai hyvin rajoittunut, isoloitu oire, vaikkapa pienialainen kipu tai muu aistivääristymä.
Koonistunut monioireinen migreeni on tyypilliseltä oirekuvaltaan aivan sama kuin miten kuvataan laaja , ”monielinoireinen” sentraalinen sensitaatio syndrooma( CSS). Akuutissa migreenikohtauksessa päänsärkyyn liittyvät tavanomaiset ennakoivat ( prodromaali -) ja jälkitilaoireet ( postdromaalioireet ) ovat migreenin kroonistuessa ”jääneet päälle” pysyviksi oireiksi ja toiminnanhäiriöiksi . Ellei migreenin patogeneesiä ja sen muuntautumiskykyä ( transformaatiota) osata huomioida, liitännäisoireista tulee ”ko-morbidisairauksia”.
Migreeni- sairauden omassa perinteisessä , osittain jo vanhentuneessa alaluokittelussa kummittelee vielä vanhojen verisuoniteorioiden pohjalta annettuja nimityksiä , kuten hemipleginen ja basillaarinen tai aivorunkomigreeni. Myös rajoittuneet ( isoloidut), kohtaukselliset ( episodiset) tai kroonistuneet päänsäryttömät migreenin ekvivalenttioireet ovat diagnostinen haaste ja altis väärintulkinnoille ja väärille hoidoille ( mm paikalliset pään alueen kivut , tukirankakivut , vapina, nykinä, voimattomuus, tinnitus, huimaus , näköhäiriöt, suoli-, rakko-, sydän-, hengitysoireet, mielialan vaihtelut )
CS:ään liittyvät sairaudet (ko-morbiditeetti)
SSS – ryhmän sairauksien ”ytimen” ovat muodostaneet useilla eri nimikkeillä tunnetut krooniset kipusairaudet ( esim fibromyalgia , entinen fibrosiitti , myofaskiaalinen kiputila, chronic widespread pain jne ), joiden perusmekanismi on ollut epäselvä ja joihin liittyy paljon muuta sairastuvuutta ( ko- morbiditeettia) , kuten depressiota , suolioireita, väsymystä . Ko-morbiditeetin lisäksi SS- sairauksia on tutkittu niitä yhdistävillä patogeneettisillä tutkimuksilla sekä erityisesti eri diagnoosi-nimikkeillä kulkevien sairauksien oirekuvausten päällekkäisellä tarkastelulla . SSS – nimikkeen tunnettavuutta ja leviämistä yleisempään käyttöön on hidastanut mm lääketieteen eri alueiden vähäinen yhteistyö . Eri erikoisaloille on kehittynyt aikojen kuluessa omia selitysmalleja tämän ryhmän sairauksille eivätkä ne aina helposti muutu. Ensimmäisten joukossa aiheesta kirjoittaneen ja oireyhtymälle tätä nimeäkin ehdottaneen Muhammad Yunuksen mukaan sentraalisen sensitaatio- syndroomaan kuuluvia sairauksia ovat mm fibromyalgia (FM) , tensiopäänsärky (TTH) ja migreeni, krooninen fatiikki (CFS) , ärtynyt paksusuoli (IBS) , monikemikaaliherkkyys (MCS) , leukanivelkipu (TMD), levottomat jalat (RLS), myofascial pain sndr (MPS) , dysmenorrhea/endometrioosi, vulvodynia, chronic regional pain syndrome (CRPS) , joiltakin osin depressio.
Ennen patogeneesin ymmärtämistä SSS -diagnooseista osaa on pidetty ns ”toiminnallisina ” tai psykosomaattisina , lääketieteellisesti selittämättöminä ( medically unexplained symptoms , MUS) tai ei sairauksina ensinkään ( non-disease)
CSS:n merkitys ja artikkeleista nousevia ajatuksia ja kysymyksiä
– CS mekanismin aiheuttamat vaivat ovat erittäin yleisiä ja saattavat olla yleisin syy lääkärissä käyntiin
– Cs tunnistamattomuus johtaa turhiin tutkimuksiin, vääriin diagnooseihin, vääriin tai turhiin lääkehoitoihin ja jopa turhiin leikkauksiin
– CS -mekanismi aiheuttamat oireet koskettavat kaikkia lääketieteen erikoisaloja
– CS-mekanismia ei opeteta lääketieteen peruskoulutuksessa, suurin osa lääkäreistä ei tunne koko termiä eikä tiedä mitä CS tarkoittaa
– CS -mekanismin kuvaus perustuu tieteelliseen neurobiologiseen tutkimukseen ja kuvantamiseen
– Monen eri sairauden tilastollisesti todettu ko-morbiditeetti selittyy yhteisellä CS-patogeneesillä
– CS-mekanismin aiheuttama sairauksien yhteinen nimitys on CSS (Central Sensitivity Syndrome)
– CSS aiheuttaa ison osan koko terveysalan kuluista
– CS:n mekanismit ovat olemassa kaikilla, yksilölliset erot taipumuksessa mekanismin ylivirittymiseen liittyvät perimään ja muokkautuminen ja kroonistuminen elämän aikana liittyy lisäksi ympäristötekijöihin
CS-mekanismi voi:
– vääristää minkä tahansa aivohermon toimintaa( esim haju,maku,näkö,kuulo,tasapaino)
– vääristää tuntohermoverkon toiminnan
– vääristää liikehermon säätelyn
– sotkea autonomisen hermoston, endokrinologisen ja hormonaalisen säätelyn tasapainon
– vaikeuttaa vireystason, uni-valverytmin, limbisen järjestelmän ja tunnetilojen säätelyä
– heikentää kognitiivisia taitoja, keskittymistä, hahmottamista
– ilmaantua ihomuutoksina tai limakalvo-oireina
– CS-mekanismi vaikuttaa koko kehon fyysiseen ja henkiseen tasapainoon
CSS- ja migreenipohdintoja:
– CS- mekanismi on keskeinen osa migreenin patogeneesiä
– Migreenin ko-morbiditeetti -tutkimuksissa nousevat esiin samat CSS -diagnoosit
– Migreenikohtauksen liitännäisoireet (prodromaali- ja postdromaalioireet ) voivat CS -mekanismin voimistuessa ja laajentuessa jäädä pitkäaikaisoireiksi
– Migreenin kroonistuessa pitkäaikaisista CS -pohjaisista oireista niistä tulee katsantokannasta riippuen joko ko-morbidisairauksia tai migreenin liitännäisoireita (ekvivalenttioireita)
– CSS on sama asia kuin krooninen monioireinen tai komplisoitunut migreeni, mutta iso osa CSS -potilaista ei tiedosta potevansa migreeniä
– CSS eli kroonisen migreenin eri oirevariaatioiden -fenotyyppien, erilaisuudet johtuvat paitsi yksilön omista geeneistä (genotyypistä), myös saman perusmekanismin anatomisesta sijainnista ja laajuudesta ja sitä kautta neurokemiallisista painotuksista
– CCS-sairauksiin toimii samat lääkkeet kuin migreeniin
– CSS- tai kroonisen migreenipotilaan oikeusturva on huono, jos hänen sairauttaan ei tunneta tai pahimmassa tapauksessa edes pidetä sairautena (Non Disease tai MUS, Medically Unexplained Symptoms). Näin voi käydä esimerkiksi päivystystilanteissa, jossa migreenikohtauksen oireita ei tunnisteta tai kroonistuneen tilanteen rappeuttaman työkyvyn arvoinnissa.
– CSS puuttuu tautinimikkeistöstä ja tämän ryhmän sairausdiagnooseilla on erilaisissa lausunnoissa huono painoarvo, lukuunottamatta ryhmään kuuluvia psykiatrisia diagnooseja kuten masennus ja ahdistus. Monet ryhmän oirediagnooseista ovat leimautuneet ”toiminnallisiksi”, psykosomaattisiksi, huolikäyttäytymiseksi tai psykiatrian termein dissosiatiivisiksi oireiksi tai jopa hypokondriaksi. Tässä yhteydessä ”toiminnallinen” on negatiivisesti latautunut termi, vaikka se on lähtökohtaisesti neutraali ilmaisu elimen hyvänlaatuiselle toiminnan vääristymiselle.
– CSS:ssa ahdistus ja masennusoireet eivät ole harvinaisia, mutta diagnooseina ne ylikorostuvat ja ovat joskus jopa turhia esimerkiksi siksi, että laajat, selittämättömät oireet tulkitaan helposti masennuksesta johtuviksi, kun CSS mekanismia ei tunneta. Masennusdiagnoosi saatetaan ottaa käyttöön sen painoarvon vuoksi esimerkiksi työkykyarvioita tehtäessä. Masennus on näistä seikoista johtuen ylidiagnosoitu sairaus.
– Varsinkin nuorten alkuvaiheen CSS / migreenin liitännäisoireet voivat olla vahvasti limbiseen järjestelmään ja emotionaaliseen säätelyyn liittyvää masennus-ahdistus oireilua. Tämä lyö helposti leimansa hoitolinjauksiin vuosiksi eteenpäin.
– Diagnoosina krooninen migreeni on myös sairauspainoarvoltaan kevyt, vaikka oireet voivat olla hyvinkin raskaita, toimintakykyä rajoittavia ja työkykyä alentavia. Migreeniin liittyviä, CS-mekanismin aiheuttamia työkykyä alentavia yleisoireista ovat esimerkiksi fatiikki, väsymys, heikentynyt rasituksen sieto ja erilaiset kognitiiviset oireet, muistin ja hahmottamisen vaikeudet.
CSS ja migreeniin merkitys terveystaloudelllisesti:
CSS sairauksien hinta koostuu:
– tutkimus – ja hoitokuluista
– turhien tutkimusten ja hoitojen kuluista
– työkyvyn arviointikuluista
– työkyvyn menetyksen kuluista
CSS / kroonisen migreenin osuus kaikesta sairastuvuudesta ja terveydenhuollon menoista on merkittävä koska:
– CSS ryhmän sairaudet ovat tavallisin lääkärissä käynnin syy (M.Yunus)
– tähän ryhmään kuuluvia sairausdiagnooseja on paljon (kts. erillinen lista)
– oireet ovat monipuolisia ja kroonisia, aiheuttavat paljon lääkärissä käyntejä
– tunnistamattomina aiheuttavat paljon eri elinsairauksien poissuljentatutkimuksia
CSS sairauksien yleisyys, esiintyvyys:
– CSS -ryhmän eri sairauksista on muutamaan diagnoosiin rajattuja ko-morbiditeetti – tutkimuksia, mutta ei tiettävästi yhteistä esiintyvyyttä selvittävää tutkimusta.
– CSS:n volyymia on mahdollista epäsuorasti hahmottaa yksittäisten sairausdiagnoosien esiintyvyysluvuilla. Kyse ei ole suorasta yhteenlaskusta, koska sairaudet ovat päällekkäisiä, saman mekanismin tuottamia erilaisia oireita.
– Laskelman pelkän päänsärkyoireen perusteella: migreeniä on 20 % :lla, TTH 80 %:lla väestöstä. Koska TTH on CS – mekanismi – ajatuksen mukaan lopulta migreeniä, on jo pelkästään päänsärkynä oirehtivan CSS:n esiintyvyys yli 80 %.
Artikkeleita migreenien syntymekanismeista
Seuraavassa pääosin lääketieteen ammattilaisille suunnattu suomennos sekä kommentointia migreenin patogeneesiä kuvaavasta artikkelista;
Migreenivaiheiden neurokemia
R Burstein, R Noseda, D Borsook ; Migraine: Multiple Processes, Complex Pathophysiology, Journal of Neuroscience, April 2015
Alkuperäisen artikkelin lääketieteellistä sanastoa on jätetty sopivan käännössanan puuttuessa ja ettei alkuperäinen merkitys vääristyisi.
Migreenivaiheet / tyypillisen migreenikohtauksen kulku ja oireet: joskus päänsärky tulee ilman varoittavia ennusmerkkejä ja päättyy nukkumalla. Jos on prodromaalioire, se voi olla fatiikki, depressio, euforia, ärtyneisyys, nälkä, ummetus, niskajäykkyys, intensiivinen haukottelu, valoarkuus, ääniherkkyys, hajuherkkyys. Jos on auravaihe, se voi olla erilaisia kortikaalisia (aivojen kuorikerrokselta tulevia) oireita, joko puutosoireita (loss of function) tai ylitoimintaa (gain of function), kuten näköhäiriö, sahalaita tai puutos aivojen takaosasta näkökeskuksesta, pistely tai puutuminen somatosensoriselta aivokuoren alueelta, toispuoleinen lihasheikkous motoriselta kuorikentältä tai tyvitumakkeista (joskus myös molemminpuoleinen lihasheikkous, joka johtunee alempien aivoalueiden alueiden häiriöstä) ja sanojen löytämisen vaikeus, afasia puhealueelta. Päänsäryn pahentuessa mukaan tulee autonomisen hermoston oireita (pahoinvointi, oksentelu, nenän sivuonteloiden turvotus, nestevuoto / rhinorrhea, kyynelvuoto, luomen roikkuminen, haukottelu, tihentynyt virtsaaminen, ripuli) mielialaoireita (affective symptoms, depressio ja ärtyneisyys), kognitiiviset oireet ( keskittymisen heikkous , sanojen löytämisen vaikeus, ohimenevä muistin heikkous, suunnistamisen vaikeus ) ja sensoriset oireet (lisääntynyt ääni, haju, valoherkkyys, lihasarkuus, ihon arkuus/ allodynia)
Migreeni on siis paljon muutakin kuin päänsärky, se on monitasoinen (complex) neurologinen vaiva (disorder), joka vaikuttaa moniin aivoalueisiin, isoaivojen kuorikerroksiin, aivorunkoon, jotka säätelevät autonomista hermostoa, mielialaa, tunteita, kognitiota, tunto – ja liikeratoja. MIgreeniaivo eroaa normaalista ja migreenin patofysiologiaa tutkittaessa on selvitettävä, miten eri aivoalueet kommunikoivat keskenään, miten ja millä mekanismeilla aivot reagoivat stressitekijöihin (unenpuute, epäsäännöllinen ruokailu, stressitilanteet ja niiden jälkitilanteet, hormonivaihtelut, alkoholi, tietyt ruuat, välkkyvä, valo, melu, tietyt hajut) ja miksi joskus migreeni alkaa ja joskus ei ala näistä ärsykkeistä. Selvitettävää on siinäkin, miksi kohtaus katkeaa itsekseen tai vain lievenee nukkumisella, rentoutumisella, ruualla, pimeällä tilalla ja millä mekanismilla episodinen migreeni tihenee ja migreeni joillakin kroonistuu.
Tautimekanismi
Monet migreenikohtaukset alkavat oireiden (prodrome, aura) perusteella aivojen keskiosista (centrally), mutta päänsärkyvaihe alkaa edellämainittujen tapahtumien seurauksena syntyvästä aktivaatiosta aivokalvojen nociceptiivisissä tuntoradoissa, jotka kuuluvat anatomisesti ns. trigeminovaskulaariseen järjestelmään/ rakenteeseen/hermoverkkoon (trigeminovascular system). On viitteitä siitä, miten aura-mekanismi voi aktivoida aivokalvojen tuntoreseptorit , mutta ei tiedetä miten edellä mainitut yleiset prodromit / ennakko-oireet aloittavat päänsäryn tai minkä tapahtumaketjun ne laukaisevat, mikä johtaa aivokalvojen tuntoreseptorien aktivoitumiseen. Geneettinen alttius tällaiseen yleistyneeseen hermoston (neuronal) ylireagoivuuteen (hyperexcitabilty) todennäköisesti on pohjalla. Usein toistuvien kohtausten seurauksena aivoissa voidaan todeta rakenteellisia ja toiminnallisia muutoksia, mikä selittäisi taudin pahentumisen ja etenemisen (progression).
a) Prodromivaihe
Tavallisimmin kuvattujen migreenin ennakoivien / prodromaali oireiden perusteella aivoalueista thalamus (fatiikki, depressio, ärtyneisyys, nälkä, haukottelu), aivorunko (lihasarkuus, niskajäykkyys), isoaivokuori (valo-ääni-hajuherkkyys) ja limbinen järjestelmä (depressio, anhedonia / ilottomuus) ovat osallisina tuottamassa migreenin oireita. Monet edellä mainituista oireista ja tuntemuksista ovat normaaleja fysiologisia ilmiöitä, mutta epäselvää on, onko nuo migreenissä ja nimenomaan migreenikolla joskus laukaisevia tekijöitä vai aistivääristymiä, jotka ovat jo jonkun tapahtumaketjun vääjäämättömiä osasia. Aivorakenteista hypothalamuksella on iso rooli kehon vuorikausirytmien (uni-valve, kehon lämpötila, nälän tunne, hormonaalinen vaihtelu) ja aivojen homeostaasin yllläpitäjänä. Migreeniaivo on hyvin herkkä homeostaasin häiriöille, joten on todennäköistä, että hypothalamuksen vrk- rytmiä ja homeostaasia säätelevät hermosolut ovat joidenkin prodromaalioireiden ytimessä tai lähtökohta. Jos pystyttäisiin ratkaisemaan, millä mekanismilla hypothalamuksen ja aivorungon hermosolut laukaisevat päänsäryn, se voisi auttaa löytämään lääkityksiä, jotka voisivat katkaista migreenikohtauksen jo prodromaalivaiheessa.
Tällä hetkellä tutkimuksen alla on kaksi pääteoriaa:
1) hypothlamuksen hermosolut, jotka vastaavat homeostaasin ylläpidosta, voivat aktivoida aivokalvojen nociceptiiviset tuntoreseptorit muuttamalla niiden parasympaattisen ja sympaattisen hermoaktivaation suhdetta parasympaattisen aktivaation (tone) suuntaan. Tähän on useita viitteitä trigeminovaskulaarisen hermojärjestelmän aktivaation aiheuttaman neurogeenisen/ -vaskulaarisen inflammation ja siihen kohdistuvan lääkehoidon tutkimuksesta. Keskeisinä aivojen tumakkeina ovat SSN, SpIN, SPG, SpV ja välittäjäaineina (neurotransmittereinä) näiden hermosolujen synapseissa ovat Ach, VIP ja NO.
2) Homeostaasin säätelyyn osallistuvat hypothamuksen ja aivorungon hermosolut voivat alentaa kynnystä kipuaistimuksen kululle thalamuksesta isoaivokuorelle. Thalamus valikoi, vahvistaa ja priorisoi informaation jota se välittää/ päästää isoaivokuorelle ja tätä järjestelmää/ hermosoluja puolestaan säätelee hypothalamuksen ja aivorungon tietyt tumakkeet. Tärkeitä valittäjäaineita näillä alueilla ovat dopamiini, histamiini, oreksiini, MCH/melanin concentrating hormone (hypothalamuksessa) sekä noradrenaliini ja serotoniini (aivorungossa). Mikä tahansa näistä välittäjäaineista voi periaattessa muuttaa thalamuksen hermosolujen vallitsevaa jännitettä (tone) ja aktivaatiota; nostaa sitä (excitatory: dopamiini, serotoniini korkealla pitoisuudella, noradrenaliini, histamiini ja oreksiini) tai alentaa sitä (inhibitory: MCH ja matalalla pitoisuudella serotoniini). Nämä eri välittäjäaineiden vastakkaiset vaikutukset selittänevät yksilöllisiä eroja ja tilannekohtaisia eroja miksi joskus ja jotkut prodromioireet liittyvät tai laukaisevat migreenin muita oireita ja miksi ulkoiset tekijät (esim. hajut) ja sisäiset olosuhteet (nälkä , unenpuute, väsymys, stressi) joskus laukaisevat migreenin.
b) CSD, Cortical spreading depression/depolarization
CSD on isoaivokuoren hermosoluissa ja gliasoluissa hitaasti etenevä jännitteen/ aktivaatiovaihtelun aalto (depolarization/excitation jota seuraa hyperpolarization/inhibition). Nykyään on vahva näyttö sille, että CSD voi laukaista migreenin auraoireen. Ei tiedetä tarkkaan ihmisillä, mikä prosessi aloittaa CSD:n. Alunpitäen jo 1940-luvulla (1944 Leao) kuvattu ilmiö on nykyään hyvin tunnettu ja pystyttä kuvantamaani ihmisillä fMRI:llä. Koe-eläinmalleissa CSD saadaan aikaan monilla ärsykkeillä, mekaanisilla ja kemiallisilla ja on spekuloitu, että monet yllä kuvatuista migreenikohtauksia laukaisevista stressitekijöistä voi sen aloittaa. Neurokemiallisesti CSD:ssä tapahtuu isoaivokuorella ensin depolarisaatiovaiheessa voimakkaana natriumin ulosvirtaus (efflux) hermosolusta sekä kaliumin ja kalsiumin sisäänvirtaus (influx) hermosoluun, glutamaatin, ATP:n ja vesi-ionien vapautuminen, hermojen turvotus (neuronal swelling), tulehdusmekanismeihin liittyvien geenien aktivoituminen ja tähän prosessiin liittyen koko joukko entsyymi-aktivaatioita (Panx1 , caspase-1) ja muutoksia mm cortexin läpäisyvyydessä. Näillä muutoksilla on puolestaan seurannaisvaikutuksia myös aivojen ulkopuolella aktivoimalla siellä tulehdusta (inflammation) mm interleukiini-1 ja high-mobility-group proteeiini-B:n sekä nuclear-factor kB välityksellä, minkä jälkeen puolestaan vapautuu aivokalvojen (subrachnoidea) tiheästi tuntohermotetulle pinnalle selkäydinnesteeseen edelleen tulehdusta aktivoivia välittäjäaineita (COX-2, NO, CGRP).
c) Aktivaatiosta sentraaliseen sensitaatioon
Migreenin kannalta keskeinen neuroanatominen alue on viidennen aivohermon (trigeminus) ja siihen toiminnalisesti läheisesti liittyvien tumakkeiden (ganglioiden) muodostama hermoverkosta ja toimintayksikkö, nimeltään trigeminovaskulaarinen (TGV) radasto. Tämän alueen migreenin kannalta tärkeät hermot kulkevat aivokalvoilta ja suurimmasta aivovaltimoista selkäytimen 5. aivohermon tumakkeeseen (nociceptive dorsal horn laminae of SpV), jossa muodostuu yhteys myös äärihermoihin silmien ympäristön iholta ja kallonpohjan lihaksista. SpV -tumakkeesta tunto- / kipuviesti kulkee aivorungon useiden tumakkeiden (PAG, formatio reticularis, SS/ superior salivary parabrachial cuneiform, nucleus solitarius) läpi hypothalamuksen tumakkeisiin (anterior, lateral, pericornial, dorsomedial, supraoptic), tyvitumakkeisiin (caudal-putamen, globus pallidus, substantia innominata). Näiden alueiden aktivaatiolla saattaa olla tärkeä rooli migreenissä pahoinvoinnin ja oksentamisen, haukottelun, kyynelvuodon, virtsanerityksen, ruokahaluttomuuden, fatiikin, ärtyneisyyden ja depression alkamiseen. SpV tumakkeesta on kytkökset on myös thalamukseen (VPM, PO,PF tumakkeet), josta puolestaan on yhteydet isoaivokuoren kivun paikkaa ja laatua, motoriikkaa, keskittymistä, muistia, näköä, kuuloa sekä hajuaisteja sääteleviin alueisiin.
d) Aktivaatio
Koeolosuhteissa CSD saa aikaan kaksivaiheisen (välitön ja viivästynyt) yllä kuvatun trigeminovaskulaarisen hermoverkoston aktivaation, joka muistuttaa tyypillistä (aurallista) migreenikohtausta. Tällainen sensitoitumisprosessi voidaan myös koeolosuhteissa katkaista lääkkeellä (M-tyypin kalium kanavan aukaisija, KCNQ2/3), joka spesifisti estää CSD:n käynnistämän nociceptoreiden aktivaation. Kuvatut havainnot puoltavat näkemysä, että migreenissä syntyy aivokalvoille neurogeeninen infalammatio, tulehduksenomainen tila, johon aivokalvojen tuntohermosäikeet reagoivat.
e) Sensitaatio
Kun trigeminovaskulaarinen hermoverkko on muuttuneen neurokemiallisen tilanteen vuoksi aktivoitunut, sen äärihermot herkistyvät / sensitoituvat (niiden ärsykekynnys, liipaisuherkkyys laskee ja vastereaktion voima kasvaa) ja ne alkavat reagoida ärsykkeille, jotka eivät synnytä reaktioita normaalitilanteessa. Kun TGV:n hermosolut tietyillä alueilla (SpV/lamin I ja V) sekä thalamuksessa (PO , VPM) sensitoituvat, niiden spontaaniaktiviteetti eli viritystaso nousee, virittynyt alue laajenee (reseptive fields expand) ja ne alkavat reagoida kivuliaasti ei kivuliaille kosketus- ja lämpöstimuluksille, jotka tulevat joko pään tai muun kehon alueelta. Kokeellisesti f-MRI kuvauksia käyttäen on kliinisiin havaintoihin sopien migreenikohtauksen etenemisestä havaittu, että kohtauksen ensimmäinen perifeeristen hermojen sensitaatio kehittyy noin 10 minuutissa ja siihen liittyy oireena sykkivä päänsärky ja paheneminen esimerkiksi kumartuessa tai yskiessä (hetkelliseen aivopaineen nousuun liittyen). Sentraalisten, aivorungon SpV tumakkeen hermojen sensitoitumiseen kuluu 30 – 60min ja sen huippu saavutetaan kahdessa tunnissa. Kliinisenä oireena on pään alueen allodynia, kevyelle kosketukselle herkistyminen sekä ihon ja lihasten arkuus. Thalamusalueen sensitaatioon menee aikaa noin 2-4 tuntia, mihin liittyy kehon muiden alueiden (extracephalic) allodynia.
f) Genetiikka, välittäjäaineet ja ylireagoiva aivo (hyperexcitable brain)
Migreenin runsas esiintyminen suvuittain viittaa vahvaan taudin geneettiseen periytymiseen. Ensimmäiset geenimuutokset, joilla oli selvä yhteys migreeniin, olivat kolme erillistä, perinnölliseen hemipleegiseen migreenin (FHM) liityvää geeniä. Nämä kaikki tunnetut FHM geenit koodaavat sellaisten proteiinien synteesiä, jotka säätelevät glutamaatin saatavuutta hermosolujen välisissä synapsiraossa. FHM1 (CACNA1A) koodaa P/Q tyypin kalsium -kanavan toimintaan liittyvää proteiinia (pore-forming alfa-1 alatyyppi), FHM2 (ATP1A2) Na/ K – ATPaasi pumpun alfa-2 tyyppiä ja FHM3 (SCN1A) Na-kanavan alfa-1 tyyppiä. Nämä geenit säätelevät välittäjäaineen eritystä, gliasolun kykyä käyttää glutamaattia synapsiraosta ja hermosolun sähköimpulssin (aktiopotentiaalin) muodostumista. Näiden 1990-luvulla löydettyjen geenimuutosten jälkeen on mm. koko ihmisen genomin kartoituksella löydetty useita migreeniin assosioivia geenejä. Myös näistä uudemmista löydetyistä geeneistä osa säätelee glutamaatin toimintaa ja osa synapsirakenteen kehitystä sekä hermojen välisen viestinnän plastisuutta.
Migreenin näkökulmasta lisääntynyt glutamaatti-välitteinen (glutaminergic) hermoaktivaatio johtaa NMDA -reseptoreiden ylikuormaan, mikä voi mahdollisesti voimistaa kipuradan toimintaa ja altistaa allodynialle ja muulle sentraaliselle sensitaatiolle. Hermoverkkoyhteyksien näkökulmasta laaja-alainen hermojen hyperaktivaatio voi olla seurausta perityn herkkyys-ominaisuuden pohjalta missä tahansa keskushermostossa (neuraxis) isoaivokuorelta thalamukseen, limbiseen järjestelmään, aivorunkoon ja selkäytimeen. Migreenissä havaitut rakenteelliset aivomuutokset voivat tästä näkökulmasta ajateltuna olla osin perinnöllisiä eikä pelkästään toistuvien kohtausten seurausta.
g) Rakenteelliset ja toiminnalliset aivomuutokset migreenissä
Fyiologisten aivotoimintamittausten perusteella on havaittu aktiviteetin nousua (terveisiin verrokkeihin nähden) seuraavilla alueilla: PAG, nucleus rubra, substantia nigra, hypothalamus, thalamuksen takaosa, pikkuaivot, insula, prefrontal cortex, ohimolohkon etuosa ja hippocampus. Alentunutta aktivaatiota somatosensorisella aivokuorella, nucleus cuneiformis, caudatum, putamen, pallidum. Nämä aktivaatiomuutokset on saatu esille yksittäisen stimuluksen jälkeen ja toistuvan stimuluksen jälkeen ginculatum ja prefrontal cortexin alueella. Nämä löydökset on tulkittu niin, että migreeniaivoilla on huono habituaatiokyky ja se tulee herkästi ylivirittyneeksi (hyperexcitable). On ollut keskustelua siitä, onko nämä ominaisuudet vain migreenissä tyypillistä . Viime vuosina on tullut paljon näyttöä siitä, että samankaltaisia muutoksia on löydettävissä muissakin kroonisissa kiputiloissa, alaselän kivussa, fibromyalgiassa, neuropaattisessa kivussa, IBS:ssa sekä ei -sydänperäisessä rintakivussa. Tämä viittaa ainakin siihen, että näissä eri fenotyypin kiputiloissa aivojen kipuprosessointi ei toimi eri tavalla.
Kliiniset havainnot migreenikohtausten ns. ekvivalenttioireista, kivusta muualla kuin päässä ja kivun ekvivalenteista (tuntohäiriöistä) ja krooniseen migreeniin aina liittyvistä muista pitkittyneistä kiputiloista on jo kauan osattu päätellä, että näitä eri nimillä kulkevia sairauksia todennäköisesti yhdistää yhteinen patogeneesi eli sentraalinen sensitaatio -mekanismi. Myös laajat epidemiologiset selvittelyt eri kroonisten kiputilojen ko-morbiditeetista viittaavat vahvasti samaan.
Anatomisesti ja rakenteellisesti MRI kuvauksilla (voxel-based morphometry – ja diffusion tensor imaging) migreenipotilailla (terveisiin kontrolleihin verrattuna) on havaittu paksuuntumista somatosensorisella cortexilla, lisääntynyttä harmaan aineen määrää caudatumissa ja harmaan aineen vähentymistä superior temporal gyres, inferior frontal gyrus, pre central gyrus, anterior cingulate cortex, amygdala, parietal operculum, middle ja inferior frontal gyrus, inferior frontal gyrus ja bilateral insula -alueilla. Monet muutokset korreloivat migreenikohtausten määrään, mutta ei tiedetä onko muutokset geneettisesti määräytyviä vai seurausta toistuvista kohtauksista tai kivusta ja stressistä. Muissakin kroonisissa kiputiloissa on havaittu samanlaisia rakenteellisia aivomuutoksia, voimakkuus korreloi sairauden kestoon ja ovat palautuvia.
Neurotransimittereiden osuus thalamuksen trigeminovaskulaari (TGV)- hermosolujen toiminnan säätelyssä migreenissä
Käännös (ja joitakin omia kommentteja ja lisäyksiä) artikkelista :
Neuropeptides and Neurotransmitters That Modulate Thalamo-cortical Pathways Relevant to Migraine Headache, R. Noseda, D. Borsook, R. Burstein, Headache 2017 ; 57: 97-111.
Thalamuksella on tärkeä rooli aivojen tiedon välityksessä. Se on kuin releasema, jonka läpi viestit sensorisesta informaatiosta kulkevat isoaivokuorelle ja tietoisuuteen. Viestejä ei ainoastaan passiivisesti ohjailla syvemmistä aivojen osista (subkortikaalisilta hermoradoilta) isoaivokuorelle (korteksille), vaan thalamuksen hermosolut ovat koko ajan aktiivisia valikoimaan, voimistamaan ja priorisoimaan miten ja minkälaisena tieto jaetaan isoaivokuorelle. Thalamus on eräänlainen aivojen portinvartija säädellessään nopeasti muuttuvaa eri puolilta aisteista tulvivaa tiedonvirtaa, antaen aivojen sopeutua jatkuvasti muuttuvaan käyttäytymisen ja ympäristöön vaatimuksiin. Säädellessään läpikulkevaa informaatiota, thalamuksen hermosoluihin kohdistuu samalla itseensä lukuisia sääteleviä (modulatory) toimintoja isoaivokuorelta, hypothalamuksesta, aivorungosta, selkäytimestä ja myös thalamuksen eri tumakkeiden välillä on keskinäistä säätelyä.
Eniten tutkittuja thalamuksen säätelytoimintoja ovat kipuaistimuksen säätely, aktivoiva (excitatory) glutaminerginen syöttö kortikothalaamiselta ja spinothalaamiselta radalta ja inhibitorinen GABA-erginen syöttö thalamuksen retikulaarisesta tumakkeesta. Aktivoiva glutamaatin, metabotrooppisen mGluR reseptorin kautta tuleva vaikutus saa aikaan jatkuvan hermovirittymisen (neuronal firing), kun taas GABA-erginen, GABA-b reseptorin kautta tuleva vaikutus sammuttaa tämän jatkuvan virityksen. Muiden thalamuksen toimintoihin vaikuttavien hermoratojen ja niissä vaikuttavien välittäjäaineiden rooli ja osuudet portinavartijana tunnetaan huonommin. Aivorungosta thalamukseen tulee serotonerginen syöttö raphen tumakkeesta, noradrenerginen locus ceruleuksesta, katekolamiini ponsista, dopaminerginen PAG:stä (periaquaductal grey) ja lateral parabrachial -tumakkeesta. Hypothalamuksesta tulee lisäksi dopaminergistä syöttöä A11ja A13 alueilta, histaminerginen tuberomammillary tumakkeesta, oreksinerginen perifornical, dorsomedial ja lateraali -alueelta ja melanin-concentrating hormooni (MCH) syöttö lateraalisesta hypothalamuksesta. Näiden monien, samoilla alueilla, samoissa synapsiraoissa vaikuttavien neurotransmittereiden rooli on oletettavasti kompleksinen, monitasoinen, osin toisiaan potentoiva tai inhiboiva tai vastasuuntaan vaikuttava ja niitä ohjaa koko joukko sisäisiä ja ulkoisia olosuhteita. Tämä säätelyjärjestelmä sopeuttaa kehon toimimaan ympäristö, tunteet ja käyttäytyminen huomioiden.
Seuraavassa tarkastellaan näiden neurotransimittereiden mahdollista osuutta thalamuksen trigeminovaskulaari (TGV)- hermoverkon toiminnan säätelyyn migreenissä. Aikaisemmissa osioissa on kuvattu tuon trigeminosvaskulaarijärjestelmän sensitoitumisen ja sen tuottaman päänsäryn ja muiden oireiden oletettu patogeneesi migreenissä.
a) Thalamuksen glutaminerginen hermotus
Thalamuksessa on suuri määrä glutamaattia sisältäviä aksoneita kaikissa trigeminovaskulaarisia hermosoluja sisältävissä tumakkeissa (VPM, Po , LP , LD). Migreenin päänsärkyyn liittyvä sensorinen aktiosignaali saapuu mm. aivokalvoilta ja kallonpohjasta kulkeutuen aivorungon C1-2 – ja trigeminuksen SpV tumakkeiden kautta trigeminothalaamista rataa thalamukseen saaden aikaan glutamaatin vapautumisen. Glutamaatti kulkeutuu synapseissa glutamaatti transportteri -vesikkeleissä (GluTs) ja vapauduttuaan aktivoi NMDA -reseptoreiden välityksellä postsynaptisia thalamokortikaalisia hermosoluja.
b) Dopaminerginen hermotus
Dopamiini sisältäviä aksoneita on kaikissa thalamuksen trigeminovaskulaarisoluja sisältävissä tumakkeissa, mutta määrältään kohtalaisesti (moderate). Dopamiinin arvellaan liittyvän migreeniin hypothalamusperäisiin oireisiin, haukotteluun ja pahoinvointiin sekä selkäytimen takasarven trigeminovaskulaaristen solujen nociseptiiviseen eli kivun säätelyyn. Thalamuksen D1- ja D2 -reseptoreiden aktivaatio osallistuu myös thalamuksen somatosensoristen VPL/VPM tumakkeiden virittymiseen (lisää membraanien depolarisaatiota ja piikkipurkausta, spike discharge) ja dopaminergiset hermot (nerve terminals) sitovat kokaiinia. Nämä seikat huomioiden on mahdollista, että thalamuksen dopamiini- hermoradat ovat osallisina lääkeaddiktiossa, impulssikontrollin säätelyssä, affekteissa, attentiossa / tarkkaavuudessa ja päätöksenteossa. Migreenin kliinisiin oireisiin liittyen thalamuksen dopamiinilla voi olla osuutta käyttäytymiseen, joka johtaa lääkkeiden liikakäyttöön, negatiivisten tunteiden päänsärkyä pahentavaan vaikutukseen, vihan ja ärtyneisyyden hallintaan, tarkkaavuutta vaativiin kognitiivisten taitoihin ja päätöksentekokykyyn.
c) Serotonerginen hermotus
Serotoniini- välittäjäainetta sisältäviä aksoneita on thalamuksen VPM ja Po tumakkeissa myös runsaasti, mikä sopii myös siihen, että serotoniinilla on jo kauan tiedetty olevan merkitystä migreenin patogeneesissä. Migreenikohtauksen triptaanilääkkeiden, serotoniini/ 5-HT 1B/1D reseptori-agonistien, tutkimustyö on selvittänyt paljon tämän välittäjäaineen roolia migreenissä. Serotonerginen rata nousee thalamukseen raphen nucleuksesta ja sen vaikutus on kaksisuuntainen, riippuen thalamuksessa erittyvän serotoniinin määrästä. Pienillä pitoisuuksilla vaikutus on aktivoiva (facilitory) ja suurilla pitoisuuksilla inhiboiva. Koska thalamuksen trigeminovaskulaarinen serotonerginen hermoverkko on hyvin tiivis ja serotoniinin pitoisuus runsas, on sen pääasiallinen vaikutus thalamokortikaaliseen informaation kulkuun lähinnä inhibitorinen. Serotoniinilla on osuutta stressin, ahdistuksen, depression, unen, ruokahalun säätelyssä sekä oppimisessa ja on luonnollista ajatella, että tämä seikka voisi liittää yhteen thalamuksen trigeminovaskulaaristen ja serotonergisten ratojen sentraalisen sensitaation ja tyypilliset migreenissä havaittavat affektiiviset ja fysiologiset häiriöt.
d) Noradrenerginen hermotus
Noradrenerginen, noradrenaliini -välitteinen radasto levittäytyy thalamuksen kaikille trigeminovaskulaarisoluja sisältäville tumakkeille, keskivahvalla tiheydellä. Se nousee aivorungon locus ceruleus tumakkeesta, joka on myös aivojen pääasiallinen tämän katekoliamiini – välittäjäaineen, noradrenaliinin tuottaja. Koska noradrenergisia hermoverkkoja on kaikkialla aivojen alueilla tiheästi, sen spesifit vaikutukset eri toimintoihin on vaikeampi määrittää. Noradrenaliini -välitteisten ratojen vaikutuksiin on liitetty laajakirjoisesti, monen mekanismin kautta, stimulusten vahvistuminen, kun siihen liittyy varautumista ja odotusta (anticipation) sekä palkitsemista (reward). Migreenissä noradrenaliini saattaa liittyä trigeminovaskulaarisolujen poikkeavaan virittymistasoon (excitability level) sekä verenpainetason säätelyyn. Beettasalpaajat (beta1- adrenoceptor blockers), jotka ovat yksi vanhimmista migreenin estolääkeryhmistä, vaimentavat thalamuksen trigeminovaskulaarisolujen aktivaatiota.
e) Histaminerginen hermotus
Histaminerginen hermotus lähtee hypothalamuksen dorsaalisesta ja tuberomammillaarisesta tumakkeesta ja on aivojen ainut histamiinin tuottaja. Histamiinia on keskivahvasti thalamuksen LP ja LD tumakkeissa ja matalia pitoisuuksia VPM ja Po tumakkeissa. Migreenissä histamiinin rooli on ajateltu olevan H1- reseptorivälitteinen vasodilataatio ja mahdollisesti siihen liittyy viivästynyt päänsärky. Keskushermostossa histamiini erittyy ainoastaan hypothalamuksen tuberomammillary -tumakkeesta, joka on aktiivinen vain valveilla ja inaktiivinen nukkuessa. Histamiini muuttaa thalamuksen rele-hermosolun jänniteastetta (discharge mode from burst to tonic) ja tämän perusteella on spekuloitu, että histaminergisen radaston moduloiva vaikutus thalamuksen trigeminovaskulaari- hermosoluihin voi liittyä migreenin ja unen yhteyksiin. Tähän liittyy tyypillinen havainto, että joskus, varsinkin lapsilla ja nuorille migreeni katkeaa unen aikana.Toisaalta, yleistä on myös vastakkainen havainto varsinkin migreenin kroonistuessa, että migreeni voi alkaa juuri yön aikana, nukkuessa. Uneen ja migreeniin liittyy myös unirytmin muutokset migreenissä, unen katkonaisuus jo migreenin prodromaalivaiheessa, sen kroonistuessa tai vastakkainen ilmiö eli liikaunisuus migreenijakson aikana. Näiden ilmiöiden takana voi olla paljon monitasoisempi, kuin pelkästään histamiinivälitteisten hermosäätöjen muutos.
f) Melanin – concentrating hormone -hermotus
Kaikissa thalamuksen trigeminovaskulaarisoluja sisältävissä tumakkeissa on MCH – radan aksoneita matalina pitoisuuksina. Tämä GABA:a sisältävä MCH-systeemi saa alkunsa lateraalisesta hypothalamuksesta ja sen moduloiva, lähinnä inhiboiva vaikutus kohdistuu energian kulutukseen, heräämiseen, liikkumiseen, seksuaaliseen kiihottumiseen ja useaan autonomisen hermoston toimintaan. Sokeritason nousu aktivoi MCH – hermosoluja, lisää GABA eritystä useilla keskushermoston tasolla ( isoaivot, aivorunko , selkäydin ) ja mahdollisesti edistää unensaantia / nukkumista ja vaikuttaa energian kulututukseen (lopettamalla ruokailun). Tämän systeemin osuutta migreenin patogeneesissä ei vielä tunneta, mutta tuoreet havainnot siitä, että hypothalaamiset MCH neuronit päätyvät thalamuksen trigeminovaskulaarineuroneja sisältäviin tumakkeisiin antaa aiheen olettaa, että esimerkiksi ruokailun, väsymyksen (drowsiness) ja migreenin yhteys välittyy osaksi näiden ratojen välityksellä. Syömisen tuoma helpotus migreenioireisiin voisi välittyä verensokerin nousun aiheuttamasta hypothalamuksen MCH neuronien aktivaatiosta ja siitä johtuvasta thalamuksen trigeminovaskulaarineuronien inhibitiosta. Saman alueen välittämänä voisi myös kehittyä tilanne toiseen suuntaan (eli migreeniä aiheuttavien tekijöiden herkistymiselle) ruokailun jäädessä väliin ja verensokerin laskiessa. Verensokerin lasku inhiboi MCH neuroneja, jolloin GABA -eritys vähenee ja thalamuksen trigeminovaskulaarineuronit herkistyvät ja ovat alttiimpia reagoimaan esimerkiksi selkäytimen trigeminus – tumakkeesta ja duran sensorisista hermoista nousevalle sensoriselle ärsykkeelle.
g) Oreksinerginen hermotus
Thalamuksen LP, LD ja mediaalisimmassa Po tumakkeen osassa on matalia pitoisuuksia, ja VPM ja lateraalisimmassa Po tumakkeen osassa on hyvin matalia pitoisuuksia oreksiinia. Näihin trigeminovaskulaarineuroneja sisältäviin thalamustumakkeisiin orexinergiset aksonit tulevat pääosin hypothalamuksen perifornical -alueesta, mutta hypothalamuksesta lähtevä orexinerginen radasto projisoituu thalamuksen lisäksi myös isoaivokuorelle, selkäytimeen ja muihin hypothalamuksen tumakkeisiin. Oreksiini-systeemissä vaikuttaa kaksi peptidiä oreksiini A ja oreksiini B, niitä tuottaa yksi sama geeni ja ne vaikuttavat kahden eri reseptorin kautta, oreksiin reseptori 1 (oreksiini A) ja oreksiini reseptori 2 (oreksiini A ja B). Oreksiini-hermosäikeiden jakauma aivoissa on laaja ja ne ovat myötävaikuttamassa ruokahaluun (food intake), heräämisen (arousal), valvetilan säätelyssä sekä sympatikus aktivaation välittämän lämpötilan nousun, sydämen syketaajuuden ja verenpaineen säätelyssä. Päinvastoin kuin MCH systeemin toiminnoissa, verensokerin laskiessa orexin neuronit aktivoituvat, mikä lisää ruokahalua ja vireyttä (vigilanssia). Kuten MCH:n, ei tämän oreksiinijärjestelmänkään osuutta migreenin patogeneesissä vielä tunneta , mutta tuoreet havainnot siitä, että oreksinergiset neuronit ovat yhteydessä migreenin kannalta tärkeisiin thalamuksen tumakkeisiin ja selkäytimen dorsaalisarven nociceptisiin laminoihin viittaavat vahvasti sen rooliin migreenimekanismeissa. Ruokailun migreenioireita helpottava vaikutus ei perustune yksin edellä kuvattuun MCH-välitteiseen, aktivoivaan GABA-vaikutukseen, vaan mahdollisesti myös inhiboivaan oreksiinivaikutukseen. Verensokerin nousu aiheuttaa oreksiini erityksen alenemisen, mikä puolestaan vaimentaa thalaamisten trigeminovaskulaari neuronien aktivaatiota. Paaston aiheuttama verensokerin lasku päinvastoin aktivoi orexinergisiä neuroneja ja lisää virittymistä (excitabilty) oreksiini A:n ja B:n välityksellä.
Sentraalisen sensitaation neurokemia
Syventävä perifeerisen ja sentraalisen sensitaation patofysiologia, ekstra- ja intrasellulaarisia näkökulmia CS:n kehittymiseen, erityisesti tähän osallistuvien hermosolujen plastisiteetin fenotyypin muutosten kuvaus mukaillen artikkelia:
Peripheral and Central Sensitization, Hazem Adel Ashmawi , George Miquel Goes Freire , Rev.dor.vol. 17 supl 1 Sao Paulo 2016.
Ennen sentraalisen sensitaation määrittelemistä yleinen käsitys kivun aistimuksesta ja säätelystä oli passiivisen prosessin omainen siten, että äärihermossa syntyneet kipusignaalit (action potentials) kuljettivat informaation paikasta, voimakkuudesta ja laadusta keskushermostoon isoaivokuorelle tietoisuuteen. Melzackin ja Wallin 1960 -luvulla esittämän porttikontrolli -teorian mukaan kipusignaalin vaimentumista tapahtui selkäytimen tasolla. Seuraavan 20 vuoden aikana löydettiin lisää näyttöä ylempien aivorakenteiden aktiivisesta roolista kivun säätelyssä, ns. inhibitorisista hermoverkoista (inhibitory nociception system). Vasta näiden havaintojen jälkeen on löytynyt vielä laajemmin keskushermostossa vaikuttava sentraaliseksi sensitaatioksi (Central Sensitization, CS) nimetty mekanismi, joka voi voimistaa kipuradan tuntemuksia monella eri tasolla ja on osallisena myös muun kuin kipuun liittyvän hermosäätelyn muutoksissa.
CS on muutos hermosolujen ja niiden muodostamien nociceptiivisten ratojen toimintatilassa koko hermoverkon (neuraxis) alueella, johtuen lisääntyneestä pintakalvon virittymisestä (membrane excitability), synapsien toiminnan tehostumisesta (efficiency) ja vähentyneestä vaimennustehosta (decreased inhibition). Useita erillisiä mekanismeja on mukana aiheuttamassa sentraalista sensitaatiota: WDR- neuronien aktivaatio (minkä seurauksena ne alkavat reagoida myös ei kivuliaisiin stimuluksiin), temporal-wind-up -ilmiö (lisääntyvä reagointi toistuvaan stimulukseen), virittyneen alueen laajentuminen sekä virittymisen jatkuminen pitempään kuin annettu stimulus. Sentraalinen sensitaatio liittyy myös hermoston plastisuuteen ja muutokset voivat olla väliaikaisia tai muuttua pysyviksi.
Sentraalinen sensitaatiomekanismi on mukana neuropaattisessa ja tulehdusperäisessä kivussa, nivelreumassa, nivelrikossa, leikkauksen jälkeisessä (pitkittyneessä) kivussa, CRPS:ssä, whiplash -oireessa, post-commotio/contusio oireissa, impingement – oireissa ja se liitetään useisiin kroonisiin kiputiloihin (pidetään niiden yhteisenä patogeneesinä), joissa ei ole pohjalla kudos- tai hermovauriota tai ei sitä pitkittyessään enää selitä, fibromyalgiassa (FM), leukanivelkivuissa (TMD), thoracic outlet syndroomassa (TOS), tenniskyynärpäässä (tenniselbow/ epikondyliitti), alaselkäkivussa (low back pain, chronic radiating low back pain/ ”pseudo-ischias”), lantion alueen kivuissa (pelvic pain, interstitial cystitis, endometriosis, vulvodynia, prostatitis), ei-sydänperäisissä rintakivuissa (noncardial chest pain), ei-elimellisissä vatsakivuissa (visceral/abdominal pain), suolistovaivoissa (IBS, dyspepsia), kroonisessa fatiikissa, masennuksessa ja ahdistuksessa, RLS:ssa, sekä migreenissä ja TTH:ssa (joka tosin on nykykäsityksen mukaan vain osa migreenin lihastensio-oiretta, sensitoitumisoiretta C2-4 dermatomilla).
Näissä luetelluissa sairauksissa on useiden epidemiologisten ko-morbiditeetti tutkimusten sekä universaalin kliinisen kokemuksen perusteella päällekkäisyyttä ja monien näiden sairauksien osalta on myös CS -mekanismin osuus sairauden patogeneesiin kokeellisesti tutkittu ja tämän ryhmän sairauksien ajatellaan edustavan erilaisia CS -fenotyyppejä, joissa korostuvat eri CS -mekanismien (vrt edellä) patogeneettiset ja neurokemialliset, mahdollisesti eri kehitysvaiheissa olevat piirteet eri anatomisilla ja toiminnallisilla alueilla, sekä mikro- (hermosolurakenteet), että makrotasolla (laajemmat elinalueet ja toiminnat).
Sentraalisen sensitaation mekanismin perusta syntyy molekulaarisella tasolla, joka seuraavassa esitetään muutaman tunnetuimman ja tärkeimmän välittäjäaineen ja reseptoreiden kautta.
Glutamaatti on tärkein hermoja stimuloiva ja sentraalisessa sensitaatiossa vaikuttava välittäjäaine, joka erittyy presynaptisesta hermosta synapsirakoon ja tarttuu useaan postsynaptiseen reseptoriin (mm. AMPAR, NMDAR, KA, mGluR). Glutamaatin ja muiden neuropeptidien, (kuten substanssi-P , CGRP) erittyessä pitemmän aikaa synapsirakooon syntyy riittävän voimakas membraanin depolarisaatio, mikä vapauttaa Mg 2+ -ionin NMDA -reseptorista, jonka tilalle glutamaatti tarttuessaan generoi sähkövarauksen ja Ca 2+ – ionien virtauksen solun sisään. Tämä voimakas kalsiumin sisäänvirtaus aktivoi monia solun sisäisiä ratoja (pathways), jotka vaikuttavat sentraalisen sensitaation ylläpitoon.
NMDA- reseptoreilla on kriittinen rooli nociceptiivisten hermojen virittymisessä (excitabilty) ja sen ohella myös glutamaatin aikaansaamalla mGlu -reseptoreiden aktivaatiolla on tärkeä rooli sentraalisen sensitaation kehittymiselle.
Samanaikaisesti glutamaatin mukana erittyvä substanssi -P (SP) tarttuu post-synaptiseen neurokinin-1 (NK1) reseptoriin (coupled to G protein) aikaansaaden pitkäkestoisen mebraanin depolarisaation.
CGRP (calsinogene related peptide), joka myös muodostuu ja erittyy tuntohermoissa, voimistaa SP:n vaikutuksia aktivoimalla proteiinikinaasi A: ta ja C: tä. CGRP lisää BDNF:n (brain- derived neurotrophic factor) vapautumista trigeminuksen nociceptiivisissä hermoissa ja on siten mukana migreenin mekanismeissa.
Bradykiniiniä, joka on inflammation syntyyn vaikuttava välittäjäaine (pro inflammatory), aktivoi ja sensitoi äärihermon (primary afferent). Bradykiniiniä erittyy myös selkäydintasolla voimakkaan perifeerisen kipustimuluksen seurauksena. Sen vaikutus välittyy selkäytimen takajuuriganglion B 2 -reseptoreiden kautta aktivoimalla proteeinikinaasi A :ta ja C.ta (PKA , PKC) ja siten nostamalla synapsien aktivaatiotatehoa (efficiency). Tähän aktivoitumismekanismin kohtaan mahdollisesti vaikuttaa myös serotonerginen laskeva rata (5-HT), 5-HT3 ja 5-HT7 reseptoreiden välityksellä.
Solunsisäisen kalsiumin pitoisuuden nousu tietyn rajan yli näyttäisi olevan sentraalisen sensitaation ensisijainen triggeri. Kalsiumin virtaus solun sisään MNDA- reseptorin välittämänä on erityisen tärkeä CS:n induktiovaiheessa. Kalsiumin sisäänvirtausta tapahtuu myös AMPA -reseptoreiden välityksellä ja myös solunsisäisellä vapautumisella mikrosomeista metabotrooppisten reseptoreiden aktivoiduttua. Lisääntynyt solunsisäinen kalsium aiheuttaa AMPA ja NMDA reseptoreiden fosforylaation (PKA/PKC:n avulla), mikä nostaa samalla näiden määrää ja aktiviteettia johtaen post-synaptiseen hypervirittymiseen (hyperexcitability). CS:n ensimmäinen vaihe on nopea virittyneiden glutaminergisten synapsien lisääntyminen selkäytimen takajuuressa, mikä vahvistaa nociseptiivistä virtausta (transmission) ja ohjaa myös ei – kivuliaan signaalin tälle hermoväylälle.
AMPAR ja NMDAR stimulaatio aktivoi myös solun sisäisiä, sentraalista sensitaatiota voimistavia ratoja, fosfolipaasi-C – (PLC ) ja PKC-, PI3K -ja proteinokinaasi ratoja. Tätä mekanismia säätelee myös extracellular signal (ERK) reseptori. ERK -aktivaatio ja fosforylaatio tapahtuu voimakkaan perifeerisen nociseptiivisen signaalin seurauksena ja joka on samanlainen mitä havaitaan CS:ssa. ERK – fosforylaatiota pidetään sentraalisessa sensitaatiossa tapahtuvan hermojen plastisuuden markkerina.
Solunsisäinen PKC -aktivaatiolla on tärkeä rooli second-order -hermon liikavirittymisessä (hyperexcitability) monellakin eri mekanismilla. Se vähentää NMDA reseptorin Mg-blokkia ja helpottaa ca-kanavien aukeamista. Aktivoitunut PKC heikentää inhibitorista hermovälitystä alentamalla GABA pitoisuutta PAG :n (periaquaductal grey ) inhibitorisissa radoissa. Tämä disinhibitio, kipusignaalia vaimentavan mekanismin heikentyminen, on tärkeä triggeri ja ylläpitäjä sentraalisen sensitaation mekanismeissa.
Yhteenvetona: Sentraalinen sensitaatio on yleinen mekanismi, joka aiheuttaa erilaisia muutoksia somatosensorisiin prosesseihin ja voi syntyä ja välittyä monin tavoin: lisäämällä kalvojännitettä (membrane excitability), lisäämällä synapsin johtavuutta tai vähentämällä inhibitorista mekanismia. CS on myös hermoverkon plastisiteettia, mutta voi tulla haitalliseksi (pathological), jos siitä tulee itsenäinen (autonomous) ja se pysyy aktiivisena ilman perifeeristä, ulkoista syytä.
Central sensitivity -syndrooma (CSS) käsitteestä
Tiivistelmä, käännös ja joitakin omia lisäyksiä artikkelista:
Muhammad B. Yunus, MD, Fibromyalgia and Overlapping Disorders: the Unifying Concept of Central Sensitivity Syndromes, 2007 Elsevier Inc, Seminar Arthritis Rheum 36;339-356.
Central sensitivity -syndroomat (CSS) käsittää ryhmän päällekkäisiä ja samankaltaisia oireyhtymiä, joihin ei liity rakenteellista poikkeavuutta ja joita yhdistää sama sentraalisen sensitaation (CS) mekanismi, jossa keskushermosto on ylivirittynyt useamman samanaikaisen synapsitason neurokemiallisen mekanismin välityksellä.
Tämän ryhmän sairauksia on usein pidetty toiminnallisina (functional), psykosomaattisina tai lääketieteellisesti selittämättöminä (medically unexplained symptoms, MUS) oireina.
CSS- sairauksille yhteisiä piirteitä on kipu, väsymys (fatiikki), huonolaatuinen uni, herkkyys kivuliaille ja myös ei-kivuliaille ärsykkeille sekä psyykkiset oireet.
CSS-ryhmän sairauksiin Yunus on listannut kuuluvaksi seuraavat sairaudet: Migreeni, TTH, IBS, CFS, FM, PTSD, FUS/IC, dysmenorrhea, MCS, PLMS, RLS, MPS, TMD. (Lyhenteiden selitykset tekstin lopussa)
Sentraalisen sensitaation mekanismi
Normaaliin kivun aistimiseen kuuluu esimerkiksi ulkoisen vamman tai tulehduksen aiheuttama perifeeristen nociceptiivisten hermojen aktivaatio ja paikallista tulehdusta synnyttävien välittäjäaineiden, kuten bradykiniinin, serotoniinin, histamiinin, prostaglandiinin ja substanssi-P (SP) erittyminen. Nociceptiiviset eli kipusignaalit kulkevat A-delta ja C-säikeitä pitkin selkäytimen takasarveen, sekä nociceptiivisiin että WDR – ( wide dynamic range) neuroneihin. A-beta säikeet kuljettavat ei-kivuliaan signaalin ja anatomisesti sekä kivuliaat että ei -kivuliaat impulssit risteytyvät, yhtyvät ( converge) WDR-neuroneissa. A-delta säikeet kuljettavat terävän ja hyvin paikantuvan kivun, joka tunnetaan first pain -nimellä. C-säikeiden kuljettama kipusignaali on tylppää, diffuusia ja polttavaa ja tunnetaan nimellä second pain. C- säikeet liittyvät krooniseen kipuun.
WDR -neuronit reagoivat laajaan kirjoon stimuluksia, kivuttomasta kevyestä kosketuksesta kivuliaimpaan. Näin WDR -neuronit integroivat risteävien kivuttomien A-beta ja kivuliaiden A-delta ja C-säikeiden informaation. A-beta säikeiden toiminta muuttuu sensitoituessa kivuliaaksi ja niiden normaalisti kivuttomana välittämä signaali, kevyt kosketus tai paine, muuttuu kivuliaaksi. Tätä ilmiötä kutsutaan allodyniaksi.
Selkäytimen postsynaptiset hermosäikeet nousevat thalamukseen, hypothalamukseen, limbiseen järjestelmään ja lopuksi aivokuorelle somatosensoriselle alueelle ja nämä kaikki eri alueet osallistuvat kivun aistimuksen, (paikan, voimakkuuden, määrään, merkityksen) prosessointiin. Kaikkien näiden tärkeiden säätöalueiden toiminta voi vääristyä sentraalisen sensitaation seurauksena. Esimerkiksi limbisen järjestelmän kivun tai sen ekvivalenttien (= vääristymien, vastineiden ) merkitystä analysoiva hälytysjärjestelmä voi kroonisessa kivussa tuottaa ahdistusoireita ja sensitoituessaan se voi laukaista ahdistus- ja paniikkioireita muunkin kuin kivuliaan aistimuksen yhteydessä (vaikkapa puutumis-pistelyoire pään alueelta tai saman sensitoitumisen tuottama kivun ekvivalenttioire tinnitus).
Sentraalisen sensitaation neurokemia
Aktivoituneet perifeeriset C-säikeet erittävät useita välittäjäaineita (neurotransmitters/neuromodulators) afferenttien eli tuovien hermosäikeiden päätteissä selkäytimessä. Nämä kemikaalit vapautuvat synapsirakoon (presynaptisen ja postsynaptisen hermon liitos), tarttuvat postsynaptisen hermon reseptoreihin ja virittävät sen. Tunnetuimpia ja sensitaation kannalta tärkeimpiä reseptoreita ovat neurokinin-1 reseptorit, joita aktivoi Substanssi -P (SP), NMDA-, AMPA- ja mGlu -reseptorit, joita aktivoi glutamaatti sekä tyrosiini kinaasi B (Trk-B) -reseptori, jota aktivoi NGF. Opioidireseptoreita on sekä selkäytimen, että muun keskushermoston alueella SP-reseptoreiden läheisyydessä, ja niiden uskotaan liittyvän SP- välitteiseen ja myös NMDA- välitteiseen neuromodulaatioon.
Substanssi-P:lla on tärkeä rooli kipusignaalin kuljetuksessa ja sen voimistumisessa (amplification) ja siten sentraalisessa sensitaatiossa. Se aktivoi synapsiraon hiljaisia reseptoreita ja osallistuu second-order -neuronin signaalin voimistamiseen (augmentation). Lisäksi SP voi kulkeutua alkuperäiseltä erittymisalueeltaan laajemmalle aiheuttaen kipualueen anatomisen laajentumisen (increased reseptive field). SP:n ja muiden välittäjäaineiden kuten glutamaatin ja NGF:n vapautuminen synapsirakoon aiheuttaa sen ylivirittymisen (synaptic hyperexcitability), magnesium – tulpan poistumisen NMDA -reseptorikanavasta, johon glutamaatti pääsee kiinnittymään ja aktivoimaan postsynaptisen hermon. Typpioksidi ( NO ) osallistuu myös tähän NMDA reseptorien aktivaatioprosessiin, mikä saa aikaan kalsiumin sisäänvirtauksen soluihin, membraanimuutoksia, proteiinikinaasien, fosfolipaasien ja NO-syntetaasin aktivaatiot sekä c-fos geenin ekspression, mitkä kaikki vaikuttavat merkittävästi sentraalisen sensitaation kehittymiseen.
NMDA – reseptorit näyttävät liittyvän keskeisesti second-order neuronien kiihtyvään ylivirittymiseen. Nämä havaittavat (phenomenal) toiminnan muutokset aiheuttavat hermojen plastisuuden, johtaen yhä voimistuvaan perifeerisen stimuluksen voimistumiseen.
Dopamiinilla on myös osuutta sentraalisessa sensitaatiossa. D1- ja D5 -reseptorit lisäävät nociceptiivista hermovälitystä, kun taas D2-, D3- ja D4- reseptorit vaimentavat sitä. Tähän sopii havainto randomoidusta kaksois-sokkotutkimuksesta, että D3-reseptori agonistilla pramipeksolilla on vaikutusta fibromyalgiassa.
Wind-up tarkoittaa progressiivista kivun aistimisen lisääntymistä, kun koe- olosuhteissa annetaan perifeeriseen C-säikeeseen nopeasti toistuva (enemmän kuin joka kolmas sekunti) stimulus. Tämä temporaalisena summaationa tunnettu ilmiö on myös tärkeä osa sentraalista sensitaatio – mekanismia ja se liittyy ”second-pain” -vaiheen kehittymiseen. Se kuvataan tylppänä, polttavana, ja se tuottaa epämiellyttävän stimuluksen jälkeisen tuntemuksen. Summaatio syntyy NMDA -reseptorien välityksellä ja se on vaimennettavissa NMDA reseptoriantagonistilla esimerkiksi ketamiinilla.
Sentraalinen sensitaatio ilmenee kliinisesti ja fysiologisesti hyperalgesiana (voimistunut kivun aistimus), allodyniana (kosketuksen aistiminen kivuliaana), kipualueen laajentumisena, pitkittyneenä hermon aktivaatiotilana stimuluksen jälkeen sekä – normaalikontrolleihin verrattuna – pitkittyneenä epämiellyttävänä jälkituntemuksena kipustimuluksen jälkeen.
Sentraaliselle sensitaatiolle ominainen, koko keskushermoston hyperviritys voi selittää herkyyden ympäristön ärsykkeille (äänet, säämuutokset, stressi) ja kemikaaleille ja lääkkeille. Sentraalinen sensitaatiolla on taipumus jäädä päälle ilman toistuvaa tai jatkuvaa stimulustakin. Se on itseohjautuvaa hermotuksen plastisuuden vuoksi ja liittyy sairauksien kroonistumiseen.
Sentraalisen sensitaation syntyyn vaikuttaa myös kehon oma vaimentava, inhibitorinen kivun säätelyjärjestelmä. Mukana on useita hermoverkkoja cortico-reticulaarijärjestelmässä, locus ceruleuksessa, hypothalamuksessa, aivorungossa sekä selkäytimessä, joissa välittäjäaineina, neurotransmittereinä ovat mm. serotoniini, noradrenaliini, GABA, enkefaliinit ja adenosiini. Nousevilla (ascending) ja laskevilla (descending) hermoradoilla ei ole vain joko stimuloiva tai inhiboiva vaikutus, vaan ne ovat enemmänkin interaktiivisia ja vaikutukset ovat kaksisuuntaisia, joko aktivoiva tai inhiboiva riippuen aktivaatiokohdasta ja välittäjäaineen alatyypistä.
Kivun affektiivinen puoli, esim epämiellyttävyys tai emotionaalinen reaktio välittyy limbisen järjestelmän sekä thalamuksen mediaalisen tumakkeen, anterior insular cortexin, anterior cingulate cortexin ja somatosensorisen kortikaalisten alueiden kautta.
Omaa pohdintaa
Kirjoittajan (Yunus) oma ensimmäinen julkaisu FM:n, IBS:n, TTH:n ja migreenin keskinäisistä yhteyksistä terveitä kontrolliryhmiä verrokkina käyttäen on vuodelta 1981 ja tämä tulos on vahvistettu myöhemmin kymmenissä muissa tutkimuksissa. Eri tutkimusten hiukan toisistaan poikkeavat esiintyvyyserot CSS -ryhmän eri fenotyyppien välillä johtuvat todennäköisimmin tutkimusten metodologisista eroista (esimerkiksi erilaisista kriteereistä taudinmäärityksessa ja alatyypityksissä), mutta CSS -sairauksien keskinäinen ko-morbiditeetti on selvästi korkeampi verrattuna julkaistuihin erillisiin väestotutkimuksiin.
Artikkelissa viitataan tutkimuksiin, jossa:
FM -syndroomaan assosioi: CFS , IBS, TTH , Migreeni, TMD, RLS, PMLS, MCS, PD, FUS, IC ja PTSD
CFS:aan assosioi: FMS, IBS, UHA ja TMD
IBS:aan assosioi: FMS, CFS ja UHA
Migreeniin assosioi: CFS ja RLS
TMD:een assosioi FMS, IBS, TTH ja IC
MCS:een assosioi FMS, CFS ja UHA
IC:een assosioi: FMS ja IBS
PTSD:een assosioi FMS ja IBS.
Kirjoittaja käy artikkelissa läpi kirjallisuusviitteitä, joissa on tutkimuksellinen, neurofysiologinen ja kuvantamisen tuoma näyttö sentraalisesta sensitaatio – mekanismista CSS-ryhmän sairauksissa; fibromyalgia (FM), chronic fatigue syndrome (CFS), irritable bowel syndrome (IBS), tension type headache (TTH), Migreeni, temporomandibular disorders (TMD), myofascial pain syndrome (MPS) / regional soft-tissue pain syndrome (RSTPS), restless legs syndrome (RLS), multiple chemical sensitivity (MCS), primary dysmenorrhea (PD), interstitial cystitis (IC), post-traumatic stress disorder (PTSD) ja depressio.
Artikkelissa pohditaan tekijöitä, jotka myötävaikuttavat (contribute) tai laukaisevat (trigger) sentraalista sensitaatiota; polygeneettisiä assosiaatioita liittyen välittäjäaineisiin, kuljettajaproteiineihin ja reseptoreihin, ulkoisia stressitekijöitä (melu, kemikaalit ym), psykologisia tekijöitä, stressiä, vammoja, infektioita sekä neuroendokrinologisen ja autonomisen hermoston säätelyn vaikutuksia.
Pohdinnassa käydään läpi eri tutkimusten välisiä metodologisia eroja myös muun kuin ko-morbiditeetin osalta. Sentraalisen sensitaation mittaamisessa käytetään lukuisia erilaisia tekniikoita ja kuvantamismenetelmiä, joista varsinkin aivojen toiminnalliset kuvaukset ovat vasta viime vuosina kehittyneet sille tasolle, että CS kyetään (tosin sekin vain viitteelllisesti lisääntyneen tai vähentyneen metabolia/ verenkierron perusteella) paikantamaan keskushermostossa anatomisesti. Erityisen vaikea on tutkia psykologisten tekijöiden osuutta tai syy-seuraus- suhteita.
Sentraalisen sensitaation, yleisen herkkyyden kehittymiseen on geneettinen taipumus. CS voi olla jo kehittynyt vielä oireettomalle henkilölle. Voimistuessaan CS johtaa oireiden syntyyn, laajentuessaan ja kroonistuessaan monioireisuuteen, CS-syndroomaan.
Pitäisikö CSS-ryhmän sairaudet yhdistää vai jakaa. Niitä yhdistää useampi tekijä kuin erottaa, mikä puoltaisi ryhmäluokittelua (group classification). Kirjoittajan mielestä ne eivät kuitenkaan ole samaa sairautta ja patogeneettiset mekanismit voivat jossakin määrin erota toisistaan.
CSS:n merkitys:
(Yunus mukaan, käännös artikkelista)
1. CSS sairaudet perustuvat biologiseen ja psykologisiin faktoihin, jolla on merkitystä ja seuraamusta potilaan ja lääkärin koulutukseen ja asialliseen hoitoon. CSS-potilaan tai potilaan oireiden todenmukaisuuden kyseenalaistaminen on perusteetonta
2. CSS – käsite luo uutta keskushermostoon liittyvää tutkimusta
3. CSS ryhmän sairauksien keskinäisen assosiaation, samanaikaisen esiintymisen ymmärtäminen helpottaa diagnostiikassa sekä auttaa välttämään turhia ja kalliita tutkimuksia ja jopa leikkauksia.
4. Koska CSS -sairauksilla on samanlaisia (mutta ei välttämättä täysin sama) patofysiologisia mekanismeja, yhden fenotyypin hoidossa löydetty toimiva lääkitys saattaa toimia myös muissa
5. CS mekanismin olemassaolo oireettomalla voi ennustaa oireisen CSS -sairauden puhkeamista tulevaisuudessa
6. CS mekanismin mukana olo elinsairauden yhteydessä (reuma, osteoartriitti, SLE) pitäisi herättää lääkärin arvioimaan myös mahdollista samanaikaista CSS -oireilua.
7. CSS:n ja elinsairauden samanaikaisuus vaatii kokonaisvaltaisen hoitosuunnitelman turhien ja haitallisten lääkitysten välttämiseksi
8. CSS ryhmän sairaudet on todennäköisesti yleisin lääketieteellinen syy, minkä vuoksi potilas konsultoi lääkäriään , joten suurempi (lääkärien) kiinnostus, akateeminen tutkimus ja rahoitus on välttämätöntä
9. Useamman samanaikaisen CSS-oireen esiintyminen potilaalla lisää CS:a ja sairauden tuomaa ahdinkoa. Hoitavan lääkärin tulisi osata huomioida ja hoitaa muutakin kuin yhtä, johtavaa oiretta
10. Eri lääkkeiden vaikutuksia CS -mekanismeihin ja potilaan oireisiin voidaan tutkia kipulaboratorioissa, ensin lähtötilanteessa, sitten lyhyissä ja myöhemmin pitkäkestoisissa kliinisissä kokeissa. Samaa testimenetelmää voidaan käyttää ei-farmakologisiin hoitoihin kuten unihygienia, kognitiivinen behavioraalinen terapia ja meditaatio
Artikkeleista nousevia ajatuksia ja kysymyksiä:
– CSS:n merkitys -yhteenveto (1-10) on erittäin hyvä ja yleispätevä
– artikkeli on reumatologin kirjoittama ja lähinnä fibromyalgian (and related disorders) näkökannalta katsottuna
– migreeni jää käsittelemättä lähes kokonaan, se on vain ”viite” tai yksi pieni osa CSS fenotyypeistä
– onko kaikki CSS kuitenkin kroonistunutta migreeniä, CSS -ryhmän sairaudet eri migreenifenotyyppejä, CS mekanismi on migreenille / migreenikolle tyypillinen synnynnäinen vääristymä (aberraatio) hermotuksen säätelyssä
– onko tarvetta, erityistä syytä pitää CSS -oireita erillään vai yhdistää ne saman nimen alle, samaksi syndroomaksi ja olisiko migreeni lähinnä sen tunnetun pitkän historiansa (satoja vuosia) vuoksi oikea nimi
– koko artikkelin voisi kirjoittaa vaihtamalla CSS-otsikon krooniseksi migreeniksi ja CS -mekanismin migreenin patogeneesiksi, eri CSS oirekuvat migreenin liitännäisoireiksi, ekvivalenteiksi, varianteiksi.